유럽인증
MDD (의료기기)
·적용 범위(Scope)
1999년 이후 유럽지역으로 수출되는 모든 의료기기는 CE마크를 부착해야 하는 강제조항이 시행되었다. 의료기기 제품인증은 안전성시험과 신뢰성시험을 통하여 제품에 대한 EU요구사항을 만족시켜야 하며, 생산시스템검증을 통한 품질경영시스템을 필요조건으로 정하고 있기 때문에 일반 제품에 대한 CE마크보다 기간이 많이 소요된다. CE/MDD마크를 취득하기 위해선, ISO 13485규격에서 규정하는 품질시스템을 수립, 운영하여야 하며, 추가적으로 MDD에서 요구하는 제품 기술 사항을 만족시켜야 한다.
의료기기 관련지침
·의료기기지침(Medical Devices Directive, 2007/47/EC)
·체외진단 의료기기지침(In Vitro Diagnostic Directive, 98/79/EC)
·능동이식 의료기기지침(Active Implantable Medical Directive, 90/385/EEC)
대표적인 Standards
의료기기 또는 체외진단 의료기기의 CE마킹을 위해서는 전 임상단계에서의 제품의 안전 및 성능에 대해 요구되는 시험을 반드시 수행하여야 한다.
그러한 시험은 대표적으로 생물학적 안전에 관한 시험 또는 전기적인 안전성에 대한 시험을 포함하여야 하며, 이에 관련된 규격은 아래와 같다.
그 외에도 제조자는 제품의 특성에 따라 관련된 요구사항을 파악하여야 하며, 이에 대한 시험을 수행하여야 한다.
·생물학적 시험 (ISO 10993 Series)
인체에 접촉 또는 삽입 되는 모든 의료기기에 대해서는, 의료기기는 생물학적 안전성 평가를 하여야 한다. 생물학적 안전성 평가는 국제 시험규격인 ISO 10993-1~20 「Biological evaluation of medical devices(의료기기의 생물학적 평가)」에 따라 수행되어야 하고, ISO 10993-1 「Evaluation and testing (평가와 시험방법)」의 틀과 원칙에 따라 의료기기의 접촉부위와 접촉시간을 고려하여 필요한 시험항목이 선택되어야 한다.
·전기 안전 시험 (IEC 60601 Series)
전기를 사용하는 의료용 전기기기 및 의료용 전기시스템은 기초 안전 및 필수 성능에 대해 EN 60601-1:2006 (IEC 60601-1:2005) Medical electrical equipment - Part 1: General requirements for basic safety and essential performance에 부합되는 시험을 하여야 하며, 개별 의료용 전기기기 별로 IEC 60601 시리즈 또는 Harmonized Standard 등에서 요구되는 추가적인 particular 규격에 대한 시험이 있는 경우, 이러한 시험이 시행되어야 한다.
·전자파 적합성(EMC) 시험(IEC 60601-1-2)
전기를 사용하는 의료용 전기기기 및 의료용 전기시스템은 전자파 적합성에 대해 EN 60601-1-2:2007 (IEC 60601-1-2:2007) Medical electrical equipment - Part 1-2: General requirements for basic safety and essential performance - Collateral standard: Electromagnetic compatibility - Requirements and tests 를 시행하여야 한다.
적합성 절차
사용 목적에 따라 결정되며 Class Ⅰ, Ⅱa, Ⅱb, Ⅲ 로 분류한다. 등급에 따라 제품의 인증절차가 다르게 적용 된다.
·Class I
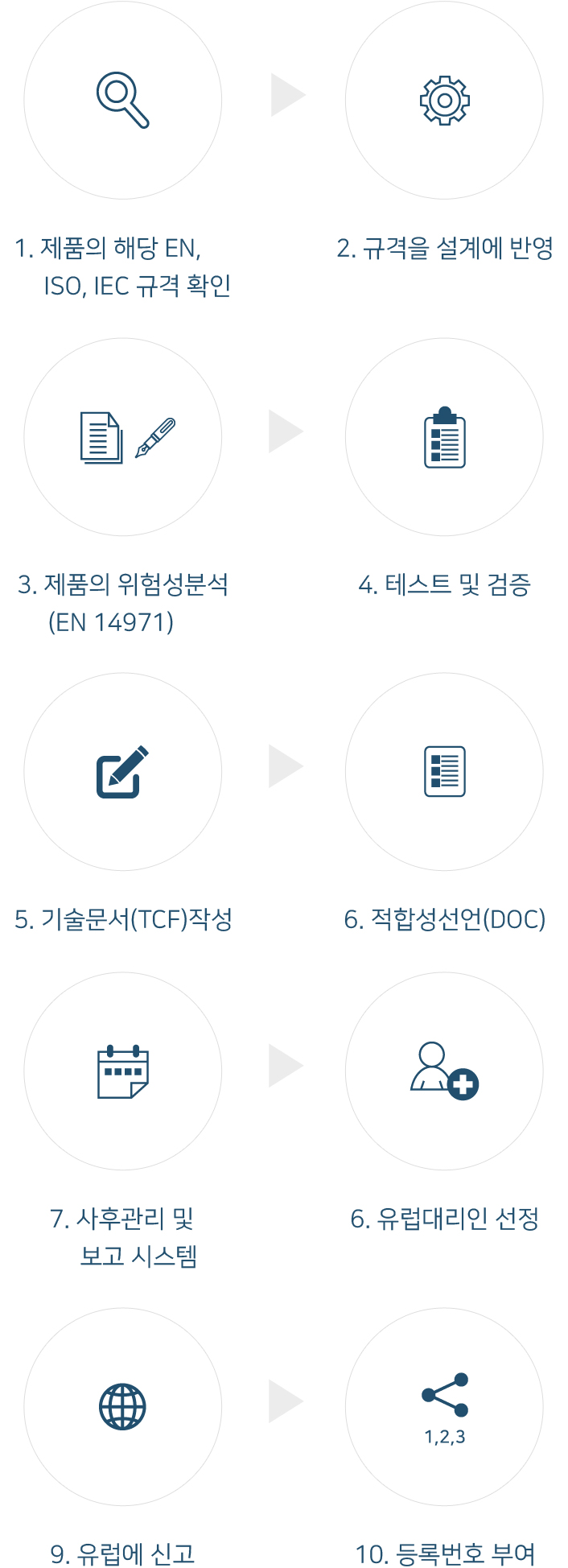
· Class IIa, Class IIb
2등급 이상의 의료기기는 1등급에 해당하는 절차에 품질시스템 인증절차가 추가된다. ISO 9001(품질보증시스템)의 규정을 따르며, 의료기기 제조업자의 특별요구사항인 ISO 13485도 충족시켜야 한다.
MDD에서는 이 규격들에 대한 규정은 없으나 대부분의 인증기관에서 이 규격의 인증을 요구하고 있으므로 이에 대한 준비를 갖추고 심사를 신청해야 한다.
IIb등급 이상의 경우에는 품질시스템 심사에 설계를 포함하는 것이 기간과 비용 면에서 유리하다. 심사는 품질시스템 구축 후 문서심사, 현장심사 순으로 진행된다. 품질시스템을 구축할 시에 무엇보다 유의해야 할 점은 제조물배상책임법(PL)에 대비하여 검사기록을 철저하게 남기고 로트에 대한 추적이 구매에서 판매까지 이루어지게 하는 작업이다. 또한 공정에 대한 유효성확인(Process Validation)을 시행하여야 하며, 가장 겉으로 드러날 수 있는 라벨링과 사용자설명서를 구성할 때도 해당 규정과 규격에 적합하도록 해야 한다.




 블로그바로가기
블로그바로가기
 본사바로가기
본사바로가기
